完善疫苗赔偿机制不仅是一个法律法规问题,也涉及到疫苗安全性跟踪这类科学问题 |
编者按
新冠的威胁,让疫苗接种几乎成为每个人不得不面临的一种抉择。
疫苗被公认为是人类对抗传染病最有力的手段,但无法完全避免的严重不良反应以及偶合事件时有发生,成为一些民众出现疫苗犹豫(vaccine hesitancy)的主要原因。例如最近网络上传言的疫苗接种后或出现白血病或I型糖尿病便引起了舆论的极大关注,即使医学专家们从专业角度解释说这些严重不良事件更有可能是偶合事件,但很多民众还是会满腹狐疑,为什么会说是偶合?
如何在这一例当中完全排除疫苗的作用?本文就来讨论一下这些极少数个案里,是如何考虑疫苗是否有关,以及疫苗伤害赔偿的问题。
撰文 | 周叶斌
责编 | 刘楚
判断严重不良反应个案
与疫苗因果关联的困难
前一篇文章(新冠疫苗导致白血病尚无证据,但疫苗安全性我们知道得也太少了!)介绍了目前国际主流药品管理部门如何通过疫苗临床试验前、人体临床试验和上市后的药物警戒以及独立的疫苗安全性跟踪系统来管理疫苗的安全性,不难看出,研究人员和监管部门的研究重点都是围绕群体水平,关注的是发生率。
可对于民众来说很多时候关注的是具体案例。比如当听到有人在接种疫苗后出现了心肌炎,我们的思考方式不会是从发生率角度——这例心肌炎属于超出自然背景值的还是在背景值范围内的,而是这一例心肌炎发生的原因是什么,与疫苗接种有没有关联。
需要强调的是,很多人可能低估了这类个案判断因果关联的困难程度。很多时候,我们必须看到,对具体的个案,我们能得出的结论会是既不能排除疫苗接种导致的可能性,也不能排除偶合。
以最近正在美国申请上市的Novavax重组蛋白新冠疫苗为例。在该疫苗的两个三期临床试验里共发生了6例心肌炎或心包膜炎,其中5例发生在疫苗接种后,1例发生在接种安慰剂后 [1]。其中,接种安慰剂后发生的那一例显然与疫苗无关,但接种疫苗后发生的5例该怎么归因呢?能否因为疫苗组发生的案例比安慰剂组更多,就认为这些是疫苗引起的吗?
没有那么简单。具体而言,虽然疫苗接种后发生了5例心肌炎或心包膜炎多于安慰剂组的1例,但这只能说是数字上的不平衡,不能确定风险是否有显著上升(即有统计学意义)。例如6例心肌炎与心包膜炎中,3例是在试验的随机双盲对照时期发生,2例在疫苗组,1例在安慰剂组。从发生率看,疫苗组是0.007%,安慰剂组是0.005%,差异并不显著。剩下3例是试验的随机双盲时期结束,安慰剂组的受试者也开始接种疫苗时发生的。而这一阶段对应潜在的自然背景病例数是1.6-4.6例,显然观察到的病例数仍然处于这一范围内。
因此,我们还没有证据说Novavax疫苗显著增加了心肌炎心包膜炎风险,更没法说疫苗组发生的病例就绝对是疫苗引发的。
那看具体的每一例情况呢?其中一例发病已经是接种第一针疫苗后的28天后,当时这位受试者又有严重的新冠感染,这似乎更有可能是病毒感染导致(心肌炎心包膜炎很多由病毒感染导致)。另外4例在接种后的10天内发生,时间上与疫苗接种更接近,但其中3例同时有病毒或细菌感染的情况,很难说心肌炎心包膜炎的发生是否与这些感染有关。
综合这些情况,美国食品药品监督管理局(FDA)给出的参考意见也只是1例 “更有可能与疫苗无关但不能彻底排除”(新冠感染那例),4例 “支持需要担心是否与疫苗存在关联”,而没法绝对判断某一例就是疫苗导致 [2]。从这个例子不难看出,由于有多种其它致病原因的存在,站在医学专业角度看一个疫苗接种后发生疾病的具体个案时,往往是很难与疫苗接种建立明确的因果关系的。
少数个案可以判断更有可能与疫苗相关
尽管大部分疫苗接种后的严重不良事件很难从个案角度去建立与疫苗的因果关系,但是在一些少数案例上,研究人员仍然可能得出结论——这个个体遇到的疾病更有可能是疫苗接种导致。
比如之前曾引起媒体广泛报道的德国一例接种mRNA疫苗后发生自身免疫性肝炎案例。截至目前大量的新冠疫苗安全性跟踪没有发现哪个新冠疫苗导致了自身免疫性肝炎或者任何一种自身免疫疾病风险上升,mRNA疫苗也不例外。甚至因为使用量大,跟踪数据完善,上市的新冠mRNA疫苗反而有更充足的证据证明没有增加自身免疫疾病的风险。可是在这例个案上,科学家倒确实找到了证据,指向这一例自身免疫性肝炎非常有可能是接种疫苗导致。
这例个案的相关研究也发表在2022年4月 Journal of Hepatology 上 [3]。一位52岁男性接种了两针新冠mRNA疫苗,每次接种两三周后都出现自身免疫性肝炎。但研究人员不是仅靠这个时间关联下结论的,而是做了非常深入的分析,探索了患者的自身免疫性肝炎机制。研究人员发现,这位患者发病的原因不同于一般自身免疫性肝炎中B细胞异常,产生攻击自身细胞的抗体,而是另一种免疫细胞——T细胞大量侵入肝脏。
到这里,研究人员只是找到了潜在 “肇事” 免疫细胞。但为什么会出现这样的肇事细胞呢?或者说有什么证据证明这些异常的免疫细胞与疫苗接种有关呢?研究人员进一步发现很多侵入肝脏的T细胞可以识别新冠刺突蛋白,这些细胞自然是疫苗接种后来的。而且血液中能识别刺突蛋白的T细胞激活程度还对应了患者的疾病严重程度。
这些都指向一种可能:在这位患者身上,疫苗接种后诱导的免疫反应出了差错,大量T细胞跑到肝脏 “干架”,形成自身免疫性肝炎——也就是人体免疫系统攻击肝脏导致损伤。
参考这例个案,我们会发现确认个案与疫苗接种的因果关系需要对该个案中的疾病发生机理做非常细致的研究。这在大部分情况下是非常困难的。比如很多病人可能没有疫苗接种前的血样,很难判断是不是在接种之前就出现了病变,只不过还没发病。又比如很多个案的发病机理研究会指向多种可能,如前文提到的Novavax疫苗临床试验里的几例心肌炎心包膜炎。
从疫苗安全性的实用角度看,更关键的还是群体水平上的风险是否增加,而不是每一例个案能否彻底明确原因。仍以自身免疫性肝炎在内的自身免疫疾病为例,这类疾病都是多种因素促成,任何一个患者发病背后都有极为复杂的遗传、环境等众多因子影响。新冠疫苗全球接种了几十亿人后,有明确的跟踪数据显示没有增加自身免疫疾病的发病率,而在这例个案上疫苗却引发了自身免疫疾病,这极可能对应了患者个人的遗传基因、个体特征甚至环境因子等复杂的 “特殊背景”。
这样的特殊性意味着此类个案不具备普适性,我们接种疫苗时的安全风险,也不由这类特殊个案决定。
疫苗伤害赔偿机制
在以上讨论疫苗罕见不良事件的因果关联分析中,可以看到即便是有明确科学证据证实疫苗增加了发病风险的不良反应,遇到具体的病例时仍然存在着属于偶合的可能性。但同时即使疫苗没有在群体水平上增加一类疾病的风险,但具体到个案时仍可能出现与疫苗接种有关的严重不良反应。
从疫苗大规模人群接种的全局去看,个案的罕见不良反应并不影响整体安全性与风险收益平衡,但另一方面对于具体罕见不良反应的受害者,更不应该忽视而应想办法给予补偿。这也是为什么我们需要不断完善疫苗伤害赔偿机制。
疫苗伤害补偿机制也是伴随着疫苗历史上标志性事件的出现而建立的。一个常被拿来参考的疫苗伤害赔偿机制是美国的疫苗伤害补偿计划,Vaccine Injury Compensation Program,简称VICP。1988年,美国国会通过了《国家儿童疫苗伤害法》,随后创立了VICP。
立法的背景是当时一些有缺陷的研究认为百白破疫苗(百日咳、白喉、破伤风混合的疫苗)可能导致神经系统疾病,一些家长据此起诉疫苗制造商。虽然绝大部分公共卫生专家认为这些诉讼没有科学依据,但一些法官更为同情家长的立场,不仅判处疫苗制造商败诉,还判了高额赔偿金。在这种威胁下,很多百白破疫苗厂商纷纷停产或表示将会停产 [4]。
而VICP设立的目的就是在对罕见的疫苗伤害事件进行经济补偿的同时,不让制造商陷入无止境的诉讼威胁。VICP带来了美国疫苗接种率的历史高位,美国每一针疫苗接种都会抽取75美分的费用给到VICP。
VICP提供了一个相对简化的疫苗伤害事件认定标准。疫苗伤害事件被分为两类。
第一类是接种疫苗已知的不良反应,如mRNA新冠疫苗的心肌炎就属于此类。属于此类的伤害事件,接种人不需要再额外举证,只需提供伤害发生在疫苗接种后一段时间内的证明即可。
第二类伤害事件是不属于疫苗已知的不良反应,那么接种人方面有举证责任。这种举证责任不是科学上证明伤害由疫苗导致,而是基于民事诉讼的原则,提供证据证明 “更有可能” 与疫苗存在因果关联即可。这里 “更有可能” 的举证标准,高于只证明了存在一种可能性,但明显低于我们在刑事案件里经常听到的 “排除合理怀疑”(beyond a reasonable doubt)[4]。
以上文提及的Novavax临床试验中发现的心肌炎案例为例,除了那例发生在接种后较久且伴随有严重新冠感染的案例(此例中更有可能是新冠感染而非疫苗导致心肌炎),其余几例大概都能符合VICP的责任认定标准。
在执行上,VICP按伤害程度做了标准化的赔偿,比如会覆盖所有的医疗支出,潜在经济损失等。
从举证标准与鉴定流程看,VICP大大简化了受害者申请补偿过程,也降低了难度。可即便如此,VICP平均每个伤害事件的鉴定时间仍然长达2年,赔偿金额(截至2007年)平均每起为85万美元 [4]。
VICP并非疫苗伤害鉴定的唯一途径,如果VCIP否决了伤害申请,接种人仍可选择向法院提起诉讼。
由于VICP设立之初是为了应对百白破这类儿童疫苗的诉讼问题,因此涵盖的疫苗主要是儿童以及孕妇接种的常规疫苗(HPV以及流感疫苗也在此列)。
而新冠疫苗属于应对大流行以及公共卫生危机采用的疫苗,赔偿会通过另一个名为CICP(Counter-measures Injury Compensation Program)的机制,天花疫苗与炭疽疫苗也属于这类 [5]。
在伤害鉴定等方面CICP与VICP是类似的。主要区别在于赔偿资金来源,VICP由每种疫苗的消费税资助,CICP的资金则来自政府拨款 [6]。
2005年12月,美国颁布了《公共准备和应急准备法》(Public Readiness and Emergency Preparedness Act,PREP Act),PREP法案授权设立美国财政基金,对符合条件的个人通过CICP机制赔偿 [7]。
中国香港特区也为新冠疫苗单列了一个10亿港币的赔偿基金 [8]。其流程与举证均类似于VICP模式,之所以专门设立一个赔偿基金,也有降低民众疫苗犹豫的考量 [9]。在香港的新冠疫苗赔偿计划里,死亡案例40岁以下赔偿金为250万港币,40岁以上为200万港币,伤害40岁以下最高赔偿金为300万港币,40岁以上为250万港币 [10]。
截至2022年5月22日,港府完成疫苗接种超过1672万剂,共有886起疫苗伤害申请,完成处理735起。其中31例死亡案例均处理完成,7例因申请个案不完整被拒绝,23例被专家委员会认为与疫苗无关或无足够信息判断,只有1例被认为 “与疫苗接种因果关系不确定”,该案例仍获得了死亡赔付,这也是至今香港唯一一起新冠疫苗接种死亡后的伤害赔付。
总结一下,已统计的855起伤害赔偿申请中,257例已获得赔偿,151例尚在处理流程中 [11]。
目前,中国内地的疫苗伤害赔偿依据主要包括《药品管理法》《疫苗流通和预防接种管理条例》以及2019年开始实施的《疫苗管理法》[12]。其中《疫苗管理法》中明确规定 “国家实行预防接种异常反应补偿制度。实施接种过程中或者实施接种后出现受种者死亡、严重残疾、器官组织损伤等损害,属于预防接种异常反应或者不能排除的,应当给予补偿” [13]。我国把疫苗接种导致的异常反应以及不能排除疫苗接种导致的情况均列入补偿范围,从疫苗伤害赔偿的基本原则看与VICP是相似的。
但不足的是,《疫苗管理法》只给出了疫苗伤害赔偿的概框架与原则,并没有建立全国统一的具体实施机制。疫苗伤害赔偿的执行仍是由各省自行负责。这就造成不同地方的鉴定标准、赔偿标准不一致,个人举证责任偏重的落实困难问题。
例如,《疫苗管理法》把 “偶合” 作为明确排除赔偿的情况 [13]。从疫苗不良反应的科学鉴定角度,这一规定是合理的。但在实践中,如何鉴别某个个案是否属于偶合是非常困难的,这在上文已有分析,因此这一规定很容易导致个体因举证难度而在行政案件中落入无法拿到伤害鉴定结果继而无法得到赔偿的困境,疫苗受害者难以得到有效救济。
从上文提及的其他国家经验可以看出,完善的疫苗赔偿机制不仅在保障少数罕见严重不良反应受害者的利益,也可以缓解疫苗犹豫。因此我国的疫苗赔偿机制改善空间还很大。
需要指出的是完善疫苗赔偿机制不仅是一个法律法规问题,也涉及到疫苗安全性跟踪这类科学问题。VICP等疫苗伤害赔偿之所以能简化鉴定赔偿流程,减轻接种人举证责任,很大程度上是由于已知罕见不良反应无需再单独举证。而这些罕见不良反应只能靠良好的疫苗安全性跟踪来不断更新。
疫苗损害作为普遍性问题,在世界各国都有发生,但目前赔偿机制较为健全的大多数是发达国家,中低收入国家的民众普遍没有这类保障。由全球疫苗免疫联盟管理的COVAX机制为92个中低收入国家建立了新冠疫苗无过失赔偿规划,是全球首创性质的尝试 [14]。
疫苗风险收益的平衡
我们确实没法排除疫苗接种后出现罕见的严重不良反应风险,我们也需要疫苗伤害赔偿来维护罕见不良反应的受害者利益。但在这些罕见不良反应的讨论中,我们不能忘记从总体的收益风险角度,去客观分析疫苗的作用。
以新冠疫苗为例,虽然多种疫苗都存在罕见的严重不良反应,但这些并不改变疫苗接种的收益远远大于风险的客观现实。
如mRNA新冠疫苗的罕见不良反应心肌炎,2021年8月美国疾控中心(CDC)做了当时的病例汇总 [15]:
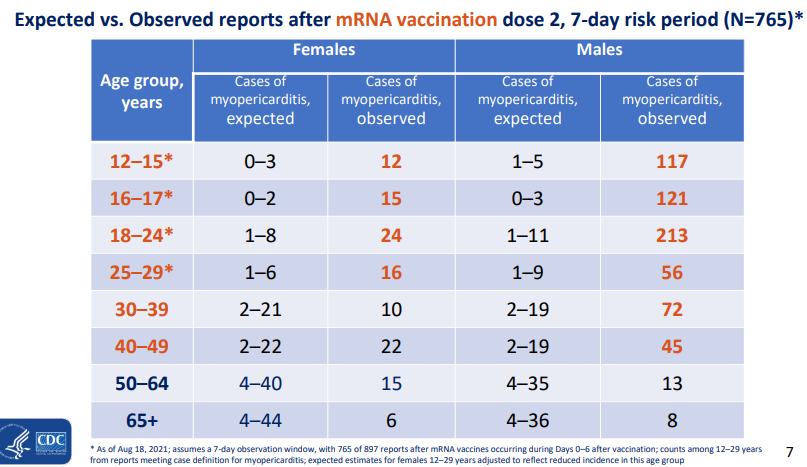
图1 mRNA疫苗罕见心肌炎不良反应的分年龄段汇总 | 图源[15]
美国疫苗不良事件追踪系统VAERS汇总了765例接种mRNA疫苗第二针后7天内发生的心肌炎病例。值得注意的是,在这个分年龄段、分性别的病例数分析中,CDC的研究人员并不是在讨论这765例是否与疫苗接种直接相关,或者区分哪些病例是疫苗导致哪些不是,而是比较接种人群男女各年龄段在7天的时间范围内,自然背景下可能发生的病例数与实际记录的病例数是否有差异。
比如在18-24岁男性中,接种人数自然背景下会发生1到11例心肌炎,而实际观察到的是213例。这个统计并没有直接得出结论说这213个相关病例中哪些属于自然背景,哪些是由于疫苗接种引起的。
换句话说,统计得出的结论不是针对某个具体个案,而是依据群体水平上的心肌炎发生率,即针对所有接种者而言,新冠mRNA疫苗增加了接种者发生心肌炎的风险,这种风险增加在年轻男性接种第二针疫苗后最为显著。
但FDA为何没有撤回该疫苗的上市许可,甚至对于接种后心肌炎风险上升最高的年轻男性,CDC仍然强烈建议接种疫苗?
原因是相比这类高效疫苗减少的潜在新冠住院、死亡,心肌炎或心包膜炎风险是极低的。根据2022年2月CDC的一个风险收益分析,18-39岁男性接种100万针Moderna新冠mRNA疫苗的第二针,在半年内可以防止1903例新冠感染引发的住院,而疫苗接种导致的心肌炎心包膜炎住院仅仅为68例 [16]:
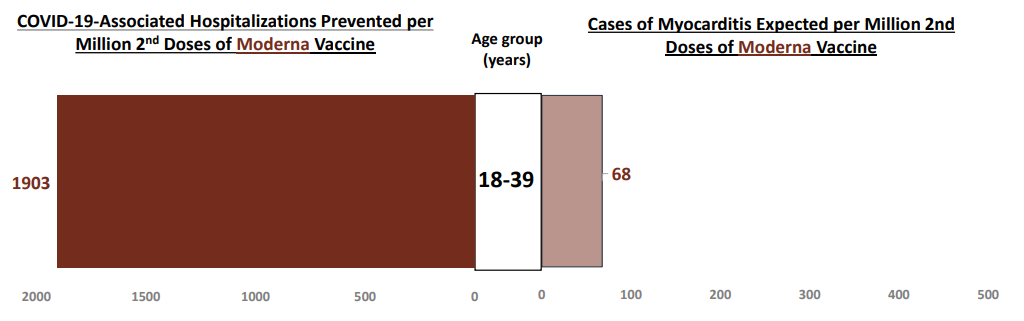
图2 新冠mRNA疫苗接种后防重症住院和心肌炎心包膜炎住院病例对比 | 图源[16]
因此,当我们关注疫苗接种带来的风险时,万万不可忽视疫苗接种的保护效果,以及不接种疫苗时存在的风险。




